Fumo sem fogo num microscópio virtual com um aumento de 100.000.000 x
Falo de um antigo truque de química sobre como mover fumo de um um canto de uma sala para outro. Vamos revelar o segredo e explicar a reacção química por detrás deste truque a um nível molecular usando um microscópio virtual com um aumento de 100.000.000 x. E finalmente a razão pela qual escolhemos esta experiência química para nosso primeiro vídeo.
Há um antigo truque de química: soprar fumo de cigarro para um copo e virá-lo ao contrário. Ao mesmo tempo, virar outro copo ao contrário no canto oposto da sala. O fumo irá viajar do primeiro copo, através da sala e aparecer no segundo copo. Tentei fazê-lo este fim de semana e passei uma boa meia hora a tossir os meus pulmões depois de um simples trago de um cigarro. Porque raio fumam as pessoas?

Então, qual o segredo por detrás deste truque?
Vamos directos ao assunto. O fumo não viaja de forma mágica para nenhum lado. Apenas acontece que enquanto que o fumo de cigarro assenta no primeiro copo, forma-se novo fumo no segundo. Existem então dois gases - cloreto de hidrogénio (o gás que, quando dissolvido em água produz ácido clorídrico) e amoníaco (aquilo a que cheira os sem abrigo). Quando misturados, estes dois gases produzem um material sólido chamado cloreto de amoníaco, cujas partículas vemos como fumo. Como já deverão ter adivinhado, é precisamente isto que acontece no segundo copo: o interior do mesmo foi coberto com uma solução aquosa concentrada de cloreto de hidrogénio (ácido clorídrico), e a mesa onde o copo foi pousado foi pulverizada com uma solução concentrada de amoníaco. Quando o copo foi pusado na mesa os dois gases começaram a misturar-se e geraram fumo.

E é este o truque. Existem várias formas de usar o efeito de fumo produzido por estes dois líquidos quando são aproximados um do outro. Começando pelo mais simples: pegue em dois cotonetes, embebam cada um deles no líquido respectivo e aproximem-nos, apreciando o efeito de criação de fumo. Ou podem pegar em dois cachimbos e impressionar o público demonstrando o fluxo de fumo de um cachimbo para outro.
Mas porque razão escolhemos esta experiência para nosso primeiro vídeo?
Inicialmente, assumi de forma pouco pensada começar pela queima de hidrogénio. Pensei que seria a reacção mais simples: o que poderá ser mais primitivo que o composto de oxigénio com o elemento mais básico - o hidrogénio? Que tolo e ingénuo estava a ser! O meu raciocínio foi: uma molécula de O2 aproxima-se de uma de H2, colidem, e se a velocidade de colisão foir superior a um determinado nível (por exemplo, se o gás estiver suficientemente quente) os átomos recombinam-se na forma mais energeticamente eficiente para formar uma molécula de H2O. Contudo, esta reacção acabou por não ser assim tão simples quanto poderia inicialmente parecer. O químico russo Nikolay Semenov e o físico inglês Cyril Norman Hinshelwood ganharam o Prémio Nobel da Química em 1956 pelas suas investigações sobre o mecanismo destas reacções químicas.
Comecei então a considerar reacções em soluções de forma a produzir precipitação. Reacções tendo por base a água são de igual forma complicadas. Os iões movem-se na água, não como partículas livres, mas antes como estruturas complexas compreendendo um ião e as moléculas de água a ele fortemente ligadas, a chamada camada de solvente. Este facto, por si só, mostra que as reacções em soluções não são tão primitivas quanto possam parecer. Não estou a falar de reacções complexas nos limites das fases, mais especificamente de uma reacção com um catalisador como este ou este.
Queríamos começar com algo simples, e então fomos pensando em várias reacções químicas e escolhemos esta, Pensámos que a geração de fumo durante uma reacção de cloreto de hidrogénio e amoníaco seria a mais facilmente compreendida e visualizável das reacções químicas.
O nosso primeiro vídeo
Existem vários vídeos bons sobre microbiologia Vídeos que mostram processos a partir de dentro. Aqui ficam vários exemplos: tradução mRNA, replicação DNA, do DNA à proteína, como o DNA é “embalado”.
Contudo, quase não existem vídeos sobre química inorgânica: quer dizer, refiro-me obviamente a vídeos que demonstrem a experiência vista de dentro, ao nível molecular e não apenas vídeos apelativos que apenas nos mostram a reacção. Agora, existe pelo menos um vídeo :) Espero que venham a existir mais em breve.
Vamos, portanto, imaginar que temos um microscópio que permite um aumento de 100.000.000 x. É este o aumento que precisamos para ver átomos. Usamos assim este microscópiio e vamos ver mais de perto:
Esta foi a primeira vez que conduzi uma experiência com os meus filhas num fim de semana e consegui mostrar-lhes o que de facto estava a acontecer no interior da reacção. Isto ajuda a perceber melhora química, melhor do que recorrendo a quaisquer fórmulas.Subscreva as nossas actualizações e siga-nos no Twitter para aprender sobre as novas experiências de química ao nosso microscópio virtual.
Problema bónus
E aqui fica o nosso problema bónus de hoje: encontre erros neste vídeo. Cometemos vários - alguns por razões artísticas, e alguns por falta de tempo. Consegue encontrá-los? Envie as suas respostas por twitter!
Veja também

Conjunto de química experimental como assinatura
Estamos finalmente prontos para dizer como será nosso primeiro produto. Será um conjunto experimental de química que você pode não usar em casa, mas não um conjunto de química tradicional. Leia quais são os três problemas que vemos nos conjuntos de química atuais e como vamos corrigi-los em nosso conjunto. Você também pode se inscrever para ser notificado quando o produto for lançado.
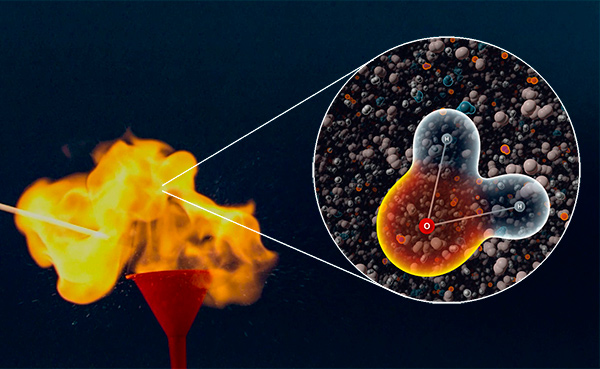
Segredos de combustão do hidrogênio
Todos nós sabemos a fórmula química da água: H2O. E a maioria de nós consegue escrever a equação da reação química que a água produz: 2H2 + O2 = 2H2O.. Mas apenas algumas pessoas em cada milhão podem explicar como esta reação ocorre na realidade. Assista ao vídeo que explica tudo.
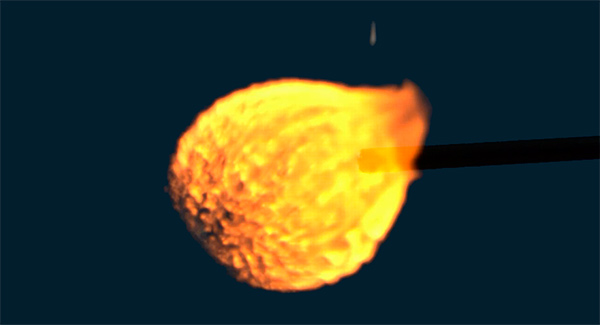
Explosões de bolhas de hidrogênio
Estamos trabalhando em um vídeo que explica o processo de queima de hidrogênio. O vídeo começa apresentando uma explosão de bolhas de hidrogênio, em seguida, aprofunda-se até o nível molecular onde é possível ver moléculas e átomos separados e entender como o processo de queima acontece. Enquanto preparamos o vídeo, filmamos muitas explosões de bolhas de hidrogênio usando uma câmera de alta velocidade. Aqui está uma compilação das melhores explosões. Aproveite! Sem ciência, só a beleza do fogo celeste :)