Знакомьтесь — металлы!
Примерно 12 тысяч лет тому назад человек нашёл необычный камень, который плавился в огне, но не раскалывался. Этот камень оказался кусочком меди. Тот день был, возможно, самым важным в истории человечества. Так началась металлическая эра, которая продолжается и по сей день. Металлы окружают нас всюду, но знаем ли мы их истинную природу и причины их необыкновенных свойств?

{Graela: Fire Assay/ CC BY-NC-SA 2.0}
##Нужно копать глубже…
В химии есть золотое правило: причина любого свойства вещества кроется в его структуре. Металлы лишь подтверждают это, ведь их структура достаточно необычна. В твёрдых телах атомы металлов заряжены положительно (назовём их ионами) и связаны друг с другом отрицательно заряженными свободно движущимися электронами. Эти электроны не принадлежат ни одному атому – они обобществлены. Для лучшего понимания представьте себе «электронный газ». Такая система из положительных ионов, связанных обобществлёнными электронами, называется металлической связью.
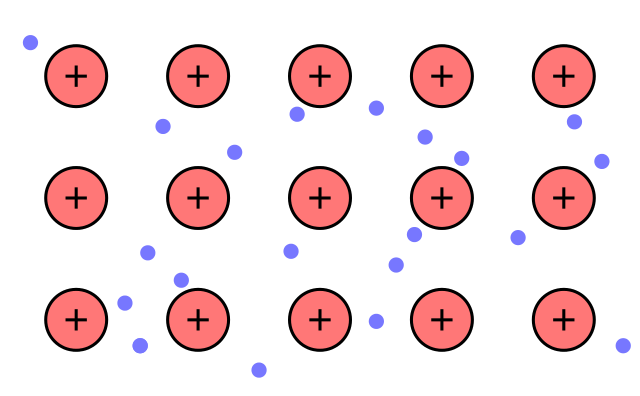
{ARTE: Модель металлической связи. Красным отмечены ионы металла, синим – электроны/ CC0}
Эта анимация отлично иллюстрирует металлическую связь:
Такая структура объясняет многие свойства металлов. Давайте рассмотрим некоторые из них подробнее.
##Металлический блеск
Металлы прекрасны прежде всего из-за их металлического блеска Именно поэтому с давних времён они используются в ювелирном деле. «Электронный газ», о котором мы говорили ранее, является причиной этого блеска. Свободно перемещающиеся электроны практически полностью отражают падающий свет, мы же воспринимаем это отражение как металлический блеск. Теперь, когда вы в следующий раз увидите прекрасное украшение, вы будете знать, почему оно так блестит!

{Serendipity Diamonds: Golden rings/ CC BY-ND 2.0}
Удивительный материал

{Barry: Forging/ CC BY-NC-SA 2.0}
Металлы зачастую пластичны. Только представьте: золотой самородок можно раскатать в лист толщиной 0,003 мм. Это возможно без разрыва металлической связи, потому что в процессе деформации свободные электроны связей сдвигаются вместе с ними. Хотя связи и сдвигаются, их очень трудно разорвать из-за их высоких энергий. Высокая энергия металлической связи также объясняет прочность металлов и их высокие температуры плавления и парообразования.
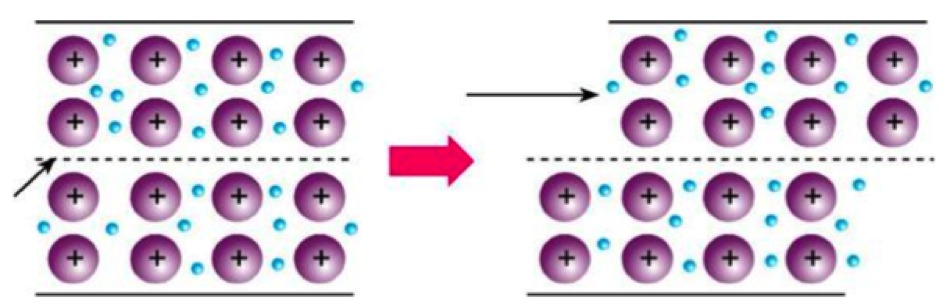
{Деформируемость металлов}
Пластичность и прочность делают металлы отличным материалом для кузнеца, ведь они ковки. Правда, при низких температурах ковкость может теряться, а металл — стать хрупким.
##Доставка тока на дом
Всем известно, что провода делают из металла, потому что металлы проводят ток. Электрическую проводимость можно объяснить с помощью теории металлической связи. Как мы уже знаем, в структуре металлов есть свободные подвижные электроны. После приложения даже небольшой разницы потенциалов эти электроны начинают перемещаться от отрицательного полюса к положительному, образуя электрический ток.

{arbyreed: Multi-line telephone cables/ CC BY-NC-SA 2.0}
##Металлы = магниты?
Мы знаем, что магниты притягивают металлические предметы. Однако, не каждый металл. Например, натрий не будет притягиваться магнитом. Дело в том, что большинство металлических предметов, которые мы используем в жизни, сделаны из железа, а оно ферромагнитно. Это значит, что ниже определённой температуры — значительно превышающей комнатную — у них появляется магнитный момент в отсутствие внешнего магнита в окружении. Этот магнитный момент является причиной притяжения металлов к постоянным магнитам. Магнитные свойства железа широко используются во многих сферах нашей жизни.
{Sarnil Prasad: Fridge magnets/ CC BY 2.0}
##Они всегда рядом
В периодической системе элементов Менделеева металлы составляют большинство: их 94 из 118 элементов. 3% нашего тела приходится на металлы, но не волнуйтесь: детекторы в аэропорту на них не сработают! Люди используют более 1,5 миллиарда тонн металла ежегодно. Мы пользуемся металлами каждый день. Благодаря их замечательным свойствам, металлы необходимы и абсолютно незаменимы в нашей жизни.
Читайте также

Вакансия – Mobile developer/product manager
Работа мечты для программиста, которому интересна мобильная разработка (iOS/Android): атмосфера стартапа (но уже без рисков и с высокой зарплатой), интересный перспективный проект с нуля с крутыми технологиями, работа на международный рынок. Задумайтесь: вы будете не просто писать очередную игру, а делать мир лучше! Такие возможности встречаются очень редко, и для вас это, возможно, станет выходом на новый виток.

Вакансия - fullstack web-developer
Привет! Мы в [MEL Science](https://melscience.com/en/v2/) ищем человека в команду, занятую всем, что связано с вебом и бизнесом: от фронтенд-оптимизаций до автоматизации полиграфии на бекенде.

Вакансия – in-house recruiter
Наши продажи активно растут (более 500% в год), растет и наша команда. Мы ищем специалиста по подбору персонала — того, кто будет заниматься поиском кадров. Успех всего бизнеса зависит от людей. Поэтому человек, организующий процесс поиска, — ключевая должность в компании.
Мы ищем очень специфичных людей, сочетающих в себе любовь к науке с умениями в своей сфере (программировать для программиста, рисовать для дизайнера и т.д.). Найти таких людей непросто, их очень мало, поэтому на некоторые вакансии мы перебираем сотни кандидатов на стадии резюме.